
¿Es el mal de Alzheimer una diabetes cerebral?
Una dieta excesiva en grasas y azúcares, sostenida por años, podría conducir directamente a la demencia. Eso es lo que sugieren los estudios de Suzanne de la Monte, neuropatóloga de la Universidad Brown de Providencia, en Rhode Island, EEUU. Han encontrado evidencias de que la insulina jugaría un rol clave en la funcionalidad cerebral, y sabiendo desde hace tiempo que una alimentación desbordada en calorías altera gravemente la producción de dicha hormona, el resultado es el mal de Alzheimer. Varios científicos han llegado incluso a cambiarle el nombre al mal de Alzheimer por el de diabetes tipo III (1).
El experimento comenzó con ratas de laboratorio. De la Monte en realidad quería estudiar el efecto del consumo de alcohol en los receptores de la insulina en el cerebro, su investigación en principio no iba dirigida al mal de Alzheimer. Su experimento consistió en interrumpir el camino de la insulina hacia las neuronas cerebrales de las ratas; el resultado fue la demencia, las ratas habían perdido la memoria, ya no encontraban el camino hacia el alimento o el agua al interior de las jaulas expresamente concebidas para experimentar con la memoria, pero además sus neuronas empezaron a recubrirse de una placa idéntica a la del mal de Alzheimer.
Representación de la molécula de insulina
La insulina es una hormona presente en muchos animales y también en el cuerpo humano. Tiene varias funciones en el intrincado organismo, la más conocida: regular la cantidad de azúcar en la sangre. La hormona da la señal a células hepáticas, musculares y grasas, de consumir la glucosa que tienen alrededor, convirtiéndola en energía o transformándola en grasa. Pero según investigaciones de hace poco más de una década, también tiene un rol importante en la regulación de ciertas funciones cerebrales que veremos más adelante.
La poca sensibilidad a la insulina es una característica de quienes padecen diabetes tipo II; con este padecimiento, las células hepáticas, lipídicas y musculares del cuerpo ya no responden a la insulina, y no ejecutan la orden hormonal de procesar la glucosa que hay alrededor. Esto hace que las tasas de insulina o de glucosa en la sangre se eleven mucho más de lo normal, con consecuencias desastrosas si no se tratan a tiempo: ataque al corazón, accidente cerebrovascular, ceguera, amputación, entre otros. La sospecha que se tiene, basada en varios análisis de laboratorio, es que el origen del mal de Alzheimer está relacionado con la misma falla de la diabetes tipo II, sólo que en este caso es el tejido cerebral el que no responde a la insulina.
El mal de Alzheimer fue descubierto por el psiquiatra y neuropatólogo alemán Alois Alzheimer hace casi un siglo, cuando seccionaba cerebros de personas que habían muerto después de varios años de demencia. Encontró que las células cerebrales (neuronas) estaban recubiertas por unas fibrillas en vastas zonas cerebrales, y que incluso varias de esas zonas tenían las células cerebrales y sus núcleos completamente desintegrados, quedando solamente las fibrillas huecas. Estudios posteriores descubrieron que esas fibrillas eran producto de la acumulación de un péptido conocido como beta-amiloide, que es el fragmento de una proteína más conocida como Proteína Precursora Amiloide, que ayuda a formar las membranas celulares en el cerebro y otras partes del cuerpo. El propio fragmento de dicha proteína, el péptido beta-amiloide tiene funciones fisiológicas demostradas en el transporte del colesterol, la regulación de ciertos genes, y la lucha antimicrobiana (es un pro-inflamatorio). Pero hasta ahora no se conocía qué factores llevan a su acumulación, formando placas que recubren las neuronas.
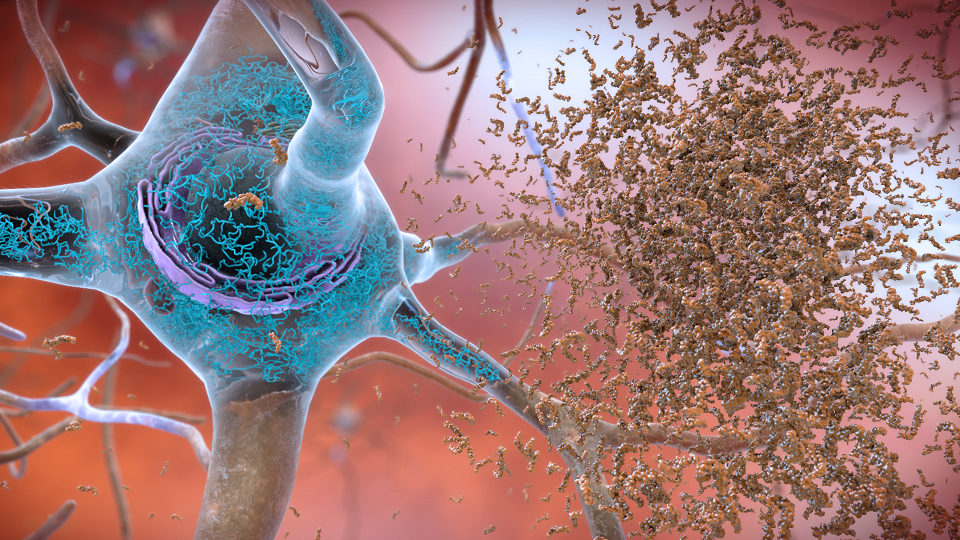
Representación de neuronas siendo recubiertas por péptidos beta-amiloides.
Imagen cortesía de National Institute on Aging/National Institutes of Health
Entre las insospechadas funcionalidades de la insulina en el cerebro se ha descubierto que: ayuda a las neuronas, sobre todo en el lóbulo frontal y en el hipocampo, a tomar la glucosa de la sangre para transformarla en energía, regula la producción de algunos neurotransmisores como la acetilcolina, vital para la contracción muscular, la memoria, la asociación de ideas y el aprendizaje, facilita la plasticidad neuronal haciendo que las neuronas tomen nuevas formas, se consoliden o creen nuevas conexiones neuronales, y colabora en buena medida con el desarrollo y funcionalidad de los vasos sanguíneos del cerebro, que aportan oxígeno y glucosa a cada rincón de la cabeza. Recordemos que el cerebro, que representa tan solo un 2% del peso total de un cuerpo humano, consume el 20% del oxígeno con que el cuerpo se abastece.
Por eso una reducción de la tasa de insulina en el cerebro tiene como consecuencia la inmediata pérdida de algunas funciones cognitivas, como la orientación espacial por ejemplo, relacionada con la memoria. Esto tiene un claro sentido evolutivo (2): cuando un animal encontraba nutrientes en algún lugar, los consumía y así la tasa de insulina en el cerebro aumentaba, reforzando la memoria del lugar donde se encontró tan energético alimento. Pero esta funcionalidad tan importante, concebida por años de evolución para adaptarse a un mundo donde había que caminar y caminar para encontrar alimento, resulta perjudicial en el mundo moderno donde el abastecimiento de alimento en algunos países está más que asegurado y hacen falta sólo algunos pasos, del living al refrigerador, para conseguir un pastelito y una gaseosa.
El sobreconsumo prolongado en el tiempo de grasas y azúcares hace que la insulina siempre se esté secretando para regular la glucosa en la sangre; al cabo de algunos años, las células parecen acostumbrarse a los altos índices de insulina y responden cada vez menos a su presencia, se vuelven resistentes a la insulina; este es el estado prediabético o diabetes tipo II, cuando no hace falta inyectarse insulina todavía pero hay que seguir una dieta estricta. Si no se cambia la dieta o no se ha descubierto una prediabetes, el páncreas se ve obligado a trabajar horas extra porque los niveles de glucosa no se reducen como antes, y las cantidades relativas de insulina y glucosa en la sangre se disparan a niveles altísimos. Luego, de un momento a otro, el páncreas tira la toalla y produce muy poca insulina: esta ya es una diabetes tipo I, con frecuencia descubierta por un coma diabético en un paciente que no se hizo a tiempo análisis de sangre para medir su glucosa sanguínea.
Si la teoría de Suzanne de la Monte es correcta, algo muy parecido sucede en el cerebro. Niveles constantemente altos de insulina, por una dieta permanentemente rica en azúcares y grasas, obligan a las neuronas a estar siempre alertas y siempre procesando la glucosa de la sangre. Con el tiempo, las células cerebrales empiezan a desobedecer la orden hormonal que da la insulina; este es el comienzo, la resistencia cerebral a la insulina, proceso paulatino que puede terminar en una indiferencia total hacia la hormona en cuestión.
La neuropatóloga no es la única en encontrar evidencia, pues se han hecho también otros experimentos en conejos y ratas de laboratorio. William Klein de la Universidad de Evanston en Illinois, EEUU, probó que provocando diabetes en conejos sus cerebros tomaban la forma de conejos con Alzheimer, con un definido aumento de proteínas beta-amiloides (3). McNay y Craft, de la Universidad de Washington, en Seattle, alimentaron ratas por un año completo con una dieta hipercalórica de azúcares y grasas; dicha dieta no sólo los condujo a contraer diabetes sino que encontraron un claro aumento de proteínas beta-amiloides en sus cerebros y comportamientos típicos del síndrome de Alzheimer como no encontrar el camino hacia su fuente de alimento en un pequeño laberinto (4).
Sin embargo, los estudios con animales de laboratorio son indicios pero no pruebas contundentes. Por eso, Steven Arnold de la Universidad de Pensilvania decidió probar la resistencia a la insulina en cerebros de cadáveres humanos, sumergiendo algunas muestras de tejido cerebral en una solución con insulina disuelta. Su sorpresa fue descubrir que los tejidos provenientes de cerebros con Alzheimer no tenían ningún tipo de respuesta, mientras que las muestras de tejido cerebral sin Alzheimer parecían resucitar por un tiempo corto al mostrar una serie de reacciones en cadena como respuesta a la insulina (5).
El mecanismo bioquímico no se conoce todavía en profundidad pero sí se conocen algunas relaciones y factores. Niveles normales de insulina en el cerebro impiden que las proteínas beta-amiloides se adhieran a las neuronas. Las neuronas cerebrales de personas con Alzheimer están atiborradas de péptidos beta-amiloides. Niveles altos de insulina bloquean la enzima que se encarga de degradar las beta-amiloides. Los péptidos beta-amiloides bloquean los receptores neuronales de la insulina, convirtiendo a dichas neuronas en resistentes a la insulina, así el cerebro necesita más insulina de lo normal, lo que bloquea todavía más la enzima que degrada los péptidos beta-amiloides, haciendo que éstas últimas se acumulen todavía más.
La acumulación de péptidos beta-amiloides puede tener varios factores, no solamente el factor insulínico. Por ejemplo, se ha demostrado que el déficit de sueño produce acumulación de péptidos beta-amiloides en el cerebro (6). Por eso no todas las personas con Alzheimer tienen diabetes declarada (aunque esté probado que muchas sí tienen problemas con la insulina sin por ello tener diabetes declarada).
A pesar de que estos estudios son más o menos recientes todavía, ya se han obtenido resultados prometedores. Craft por ejemplo, realizó un estudio (7) con más de 100 voluntarios a quienes se les siguió un tratamiento por spray nasal de insulina. Los resultados fueron significativos: una mejora en la memoria, una capacidad aumentada de atención, y un autocuidado mejorado. También se abren otras lineas de investigación para tratar de curar o al menos frenar el avance del Alzheimer probando los fármacos actualmente usados para tratar la diabetes. De todos modos, si se quiere prevenir, la mejor opción será cuidar la alimentación y no ingerir grasas y azúcares en exceso, y hacer ejercicio varias veces por semana, eso si se quiere tener no solamente un cuerpo sano, si no también una mente sana.
Estos estudios resultan alentadores para la investigación del mal de Alzheimer, pero no es una buena noticia para quienes padecen diabetes tipo II porque tendrían un factor de riesgo mayor de contraer ese mal. Sumémosle a esto la dieta de gaseosas, dulces, hamburguesas, mayonesa o papas fritas que tienen a una parte de la humanidad luchando contra la obesidad, y estaríamos encaminados directamente a una explosión de casos de mal de Alzheimer producto de ya varias decenas de años de una mala alimentación.

Autorretratos del pintor William Utermohlen, las dos primeras pinturas cuando su cerebro todavía estaba sano, el resto, cuando ya padecía Alzheimer.
Si se llega a demostrar que el mal de Alzheimer es producido en gran parte por una mala alimentación con grasas saturadas, exceso de carbohidratos y azúcares, se estaría ayudando a poco más de 50 millones de personas en el mundo que padecen esa enfermedad hoy en día, porque se abrirían nuevos frentes para combatirla, con tratamientos para ayudar al tejido cerebral a responder correctamente a la insulina, y también para evitar que millones más contraigan el mal a través de dietas alimenticias recetadas a tiempo.
Investigación y Redacción: Álvaro J. Riquelme Marinkovic
Fecha de publicación: 19-11-2020
Última actualización: 19-11-2020
Producido en: Valdivia - Chile
Fuentes:
(1) de la Monte, S. M., & Wands, J. R. (2008). Alzheimer's disease is type 3 diabetes-evidence reviewed. Journal of diabetes science and technology, 2(6), 1101–1113. https://doi.org/10.1177/193229680800200619
(2) Bijal Trivedi – Eat your way to dementia – New Scientist 09-2012
(3) Bitel CL, Kasinathan C, Kaswala RH, Klein WL, Frederikse PH. Amyloid-β and tau pathology of Alzheimer's disease induced by diabetes in a rabbit animal model. J Alzheimers Dis. 2012;32(2):291-305. doi: 10.3233/JAD-2012-120571. PMID: 22785400.
(4) McNay, Ewan & Green, Pattie & Craft, Suzanne. (2010). Type 2 diabetes and recurrent hypoglycemia both elevate hippocampal amyloid, but by different mechanisms. Alzheimers & Dementia - ALZHEIMERS DEMENT. 6. 10.1016/j.jalz.2010.05.681.
(5) Konrad Talbot, Hoau-Yan Wang, Hala Kazi, Li-Ying Han, Kalindi P. Bakshi, Andres Stucky, Robert L. Fuino, Krista R. Kawaguchi, Andrew J. Samoyedny, Robert S. Wilson, Zoe Arvanitakis, Julie A. Schneider, Bryan A. Wolf, David A. Bennett, John Q. Trojanowski and Steven E. Arnold. Demonstrated brain insulin resistance in Alzheimer’s disease patients is associated with IGF-1 resistance, IRS-1 dysregulation, and cognitive decline. Journal of Clinical Investigation, 2012 DOI: 10.1172/JCI59903
(6) Jessen NA, Munk AS, Lundgaard I, Nedergaard M. The Glymphatic System: A Beginner's Guide. Neurochem Res. 2015;40(12):2583-2599. doi:10.1007/s11064-015-1581-6
(7) Craft, Suzanne & Claxton, Amy & Baker, Laura & Hanson, Angela & Cholerton, Brenna & Trittschuh, Emily & Dahl, Deborah & Caulder, Erin & Neth, Bryan & Montine, Thomas & Jung, Youngkyoo & Maldjian, Joseph & Whitlow, Christopher & Friedman, Seth. (2017). Effects of Regular and Long-Acting Insulin on Cognition and Alzheimer's Disease Biomarkers: A Pilot Clinical Trial. Journal of Alzheimer's disease : JAD. 57. 10.3233/JAD-161256.
